
Главная страница Случайная страница
КАТЕГОРИИ:
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Розрахунок молярних мас еквівалентів хімічних речовин
|
|
За рекомендацєю ЮПАК еквівалентом називають реальну або умовну частинку речовини, яка в даній кислотно-основній реакції еквівалентна одному іону водню або одному електрону в реакції окиснення-відновлення. При використовуванні поняття “кількість еквівалентів речовини” завжди необхідно вказувати, до якої конкретної реакції воно відноситься. Одиницею вимірювання еквівалентної кількості речовини (neq) є моль, наприклад, n(H2SO4)eq; n(KMnO4)eq.
Молярна маса еквівалента речовини М(В)eq – це відношення маси речовини m(В) - до кількості еквівалентів речовини n(В)eq, що відповідає даній масі.
M(B)eq = 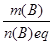 , г/моль.
, г/моль.
де n(В)eq - кількість еквівалентів речовини (В), моль;
m(В) - маса речовини (В), г.
Мeq складної речовини змінюється в залежності від того, в яку хімічну реакцію вступає дана речовина.
Наприклад, молярна маса еквівалента фосфорної кислоти дорівнює молярній масі кислоти, поділеній на число моль іонів водню, заміщенних у кислоті на катіон металу в даній реакції:
а) Н3РО4 + КОН = КН2РО4 + НОН
М(Н3РО4)eq = 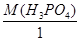 =
=  98 г/моль
98 г/моль
б) Н3РО4 + 2КОН = К2НРО4 + 2НОН
М(Н3РО4)eq = 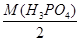 = 49 г/моль
= 49 г/моль