
Главная страница Случайная страница
КАТЕГОРИИ:
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Механизм сопряжения дыхания и фосфорилирования в митохондриях 4 страница
|
|
3. Бесхлорофильнын фотосинтез
Бесхлорофильиый фотосинтез обнаружен у солелюбивых бактерий, имеющих фиолетовый светочувствительный пигмент. Этим пигментом оказался белок бактериородопсин, содержащий, подобно зрительному пурпуру сетчатки — родопсину производное витамина А — ретиналь. Бактериородопсин, встроенный в мембрану солелюбивных бактерий, образует на этой мембране в ответ на поглощение ретин ал ем света протонный потенциал, преобразующийся в АТФ. Таким образом, бактериородопсин является бесхлорофнльным преобразователем энергии света.
4. Фотосинтез и внешняя среда
Фотосинтез возможен только при наличии света, воды и диоксида углерода. КПД фотосинтеза не более 20% у культурных видов растений, а обычно он не превышает 6—7%. В атмосфере примерно 0, 03% (об.) COs, при повышении его содержания до 0, 1%' интенсивность фотосинтеза к продуктивность растений- возрастают, поэтому целесообразно подкармливать растения гндро- карбонатами. Однако содержание СОг в воздухе выше 1, 0% оказывает вредное действие на фотосинтез. За год только наземные растения усваивают 3% всего С02 атмосферы Земли, т. е. около 20 млрд. т. В составе синтезируемых нз С02 углеводов аккумулируется до 4 • 1018 кДж энергии света'. Это соответствует мощности электростанции в 40 млрд. кВт. Побочный продукт фотосинтеза— кислород—жизненнд необходим для высших организмов и аэробных микроорганизмов. Сохранить растительный покров — значит сохранить жизнь на Земле.
В. ОБМЕН ВЕЩЕСТВ
ГЛАВА 17. ОБМЕН УГЛЕВОДОВ
Превращение углеводов в тканях организма складывается из ферментативных процессов, ведущих к распаду углеводов (катаболнческие пути) или их синтезу (анаболические). В ходе распада углеводов освобождается энергия или образуются необходимые для других биохимических процессов промежуточные продукты. Синтез углеводов служит для восполнения запасов резервных полисахаридов или обновления структурных углеводов. Мощность различных путей обмена углеводов в тканях и органах определяется наличием в них соответствующих ферментов.
пентозофосфатный цикл называют циклом Варбурга—Диккенса—Хорекера— Энгельгардта.
Пентозофосфатный цикл представляет собой полиферментную систему, где важным промежуточным продуктом, судя по названию, служат пентозо- фосфаты. Этот цикл является как бы ответвлением, или шунтом, гликолиза на стадии глюкозо-б-фосфата.
Пентозофосфатный цикл
Для протекания всех стадий пентозофосфатного цикла требуется не менее трех молекул глюкозо-б-фосфата. Рассмотрим отдельные реакции этого цикла.
1. Дегидрирование глюкозо-6-фосфата — реакция, направляющая глю- коэо-6-фосфат по пентозофосфатному пути, катализируется гмокозо-6-фосфат- дегидрогенаэой по уравнению (для полного описания циклического процесса в уравнениях реакций сразу используем три молекулы глюкозо-6-фосфата)
| \ с--- I н—с—он I з но—с—н |
| '---- 1 н—С—ОН но—с—н о н—с—он H-f-------- 1 Н, с—OPO.H, |
| 9 юл> -6-фосф»т-дег |
| HjC—OPOjKj Ил юк озо-6-фосфат |
Дегидрогеназа глюкозо-б-фосфата — димер с молекулярной массой около 135 ООО. Имеется 7—8 изоферментов этого фермента, разделяющихся при электрофорезе. Особенностью этой реакции является образование НАДФ • Н2. Равновесие реакции сильно сдвинуто вправо, потому что образующийся лак- тон или спонтанно, или с участием лактоназы гидролизуется.
2. Гидролиз 6-фосфоглюконолактоца с образованием 6-фосфоглюконата:
| н—i—он I 3 но—с—н н—(i—он hJ- |
| н-i-o[4] " lrn" t"» з но—d: —н t3H, 0 I H—С—он „X |
Н, С—ОРО, Н2
| i-o |
| Hgi |
б.фосфоглоюмт
3. Дегидрирование 6-фосфоглюконата с образованием рнбулозо-5-фосфа-
| t |
та. Эта реакция катализируется 6-фосфоглюконат-дегидрогеназой по уравнению
соон
I
н—с—он
I
3 но—с—н
н—< j: —он
н—с—он
I
н2с—ого3н2
& -фосфоглююмат
Равновесие реакции сдвинуто вправо. б-Фосфоглюконат-дегидрогеназа—ди- мер с молекулярной массой около 100 000. Имеется несколько изоферментов этой дегидрогеназы. Особенность реакции состоит в том, что при дегидрировании образуется нестойкое промежуточное соединение, которое на поверхности этого же фермента декарбоксилируется. Это вторая реакция окисления в пентозофосфатном цикле, приводящая к образованию НАДФ • Н2, поэтому превращение глюкозо-6-фосфата до рибулозо-5-фосфата принято называть окислительной фазой пентозофосфатного цикла. Фаза от рибулозо-5-фосфата до образования вновь глюкозо-6-фосфата называется неокислительной или анаэробной фазой этого цикла.
4. Взаимопревращение, или изомеризация, пеитозофосфатов. Рибулозо- 5-фосфат может обратимо изомеризоваться в другие пентозофосфаты — кси- лулозо-5-фосфат и рибозо-5-фосфат. Катализируют эти реакции два разных фермента — пентозофосфат-эпимераза и пентозофосфат-изомераза по уравнениям:
н, с—он н„с—он
< i-o < i-o
I П«атсаофосфат I Певтоаофосфат- |
2 НО—С—H миррам, 3 Н—С—ОН иомерам | Н—С—ОН
н—(?: —он н—(?: —он н—<!: —он
—■ OPOjHJ Hjti—opOjHj Hjd—OPOJHJ
D - ксилулоэ о -S -фосфат D- р кбул оао-5-фосфат
D -ревою- 5-фосфат
I
н—с—он
Образование из рибулозо-5-фосфата двух других пеитозофосфатов — рибозо 5-фосфата и ксилулозо-5-фосфата необходимо для последующих реакций цикла. Причем требуется две молекулы ксилулозо-5-фосфата и одна молекула рнбозо-5-фосфата.
| Г0 3 н—С—ОН +3CO, I Н—С—ОН Н, С—OPOjH, |
| D- pw було jo-5-ф осфат |
5. Перенос гликодевого альдегида с ксилулозо-5-фосфата на рнбозо-5- фосфат, или первая трансхетолазнан реакция. В следующей реакции, катализируемой транскетолазой, используются образовавшиеся в предыдущей реакции пентозофосфаты (в рамку взят переносимый фрагмент):
Н2С—ОН! н—с-о! с = о!
I I 1 и-т—
__с=о_ | Н—с—он но—с—н н—с=о
1—1—Н 4- H-tt—ОН Jfygszy'??, Н-С—ОН + н-с—о. 1-е—он н-^-он м? 1+ H-d-ои Hs< i-o.
Hjd—opo, Hj н, с—.оро, н, н—с!; —он
i
hjc—0p03hs dmime
В транскетолазной реакции расходуются молекулы рибозо-5-фосфата и одна из двух молекул ксилулозо-5-фосфата. Другая молекула используется позднее, во второй транскеголазной реакции.
Транскетолаза — димер с молекулярной массой 140 000. Коферментом ее является тиаминдифосфат. Реакция требует ионов Mg2+. Оба продукта транскетолазной реакции используются на следующей стадии цикла в качестве субстратов.
6. Перенос дигидроксиацетонового фрагмента с седогептулозо-7-фосфата на глицеральдегид-3-фосфат. Эта обратимая реакция катализируется траке- альдолазой по уравнению
> Н2С—он
; Lo.
Н—С—он
I
н—с—он I
| ЬН-А- |
н-с—он hs< -; —opo3hs
н2с—он]
и!
но—d: —н J н—J—он
н—с—он I
hjc—орозн,
13 фруктозе 6-фосфаг
H—С = 0
н—d—он h н—(!: —он н5с—ор6, н}
Трансальдолаза — димер с молекулярной массой около 70 000. Молекула фруктозо-6-фосфата, образующаяся в этой реакции, подключается к гликолизу, а эритрозо-4-фосфат используется как субстрат для последующих стадий цикла.
7- Перенос гликолевого альдегида с ксилулозо-5-фосфата на эритрозо-4- фосфат, или вторая транскетолазная реакция. Эта реакция сродни первой транскетолазной реакции и катализируется тем же ферментом. Отличие ее в том, что акцептором гликолевого альдегида служит эрнтрозо- 4-фосфат:
U--Q
-j- J н—d; —.
НО—С—Н + I Tp.HcitCTG< .»»t НО—С—Н I
I H-d-он " ------ I + н-с-
н—С—ОН I н—С—г-
I HtC—OPO.H, I
| н-с=о |
| —ОН H, fc—OPOjH, |
HSC—OPOjH, Н—С—<
Hi-
5-фосфат Дмфаг' HjC—OPOjHj
Фруктозо-б-фосфат и глнцеральдегид-3-фосфат подключаются к гликолизу.
Следовательно, в ходе реакций, катализируемых собственно ферментами пеитозофосфатного цикла, из трех молекул глюкозо-6-фосфата образуется две молекулы фруктозо-6-фосфата, одна молекула глнцеральдегнд-3-фосфата и три молекулы диоксида углерода. Кроме того, образуется шесть молекул НАДФ • Н2. Суммарное уравнение пеитозофосфатного цикла:
ЗГлюкоэо-6-фосфат + 6НАДФ+ -*■ 2Фруктозо-6-фосфат + Глицеральдегвд-З-фосфат +
+6НАДФ-Ц + 3COs
Взаимосвязь пеитозофосфатного цикла и гликолиза
Оба пути превращения углеводов тесно связаны (рис. 49). Продукты пеитозофосфатного пути — фруктозо-б-фосфат и глицеральдегид-3-фосфат — являются также метаболитами гликолиза, поэтому они вовлекаются в гликолиз и превращаются его ферментами. Две молекулы фруктозо-6-фосфата могут регенерироваться в две молекулы глюкозо-6-фосфата с помощью глюкозо- фосфатнзомеразы — фермента гликолиза. В этом случае пентозофосфатный
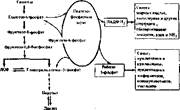 Рис. 49. Схема интеграции вентозофосфатиого шунта с гликолизом
Рис. 49. Схема интеграции вентозофосфатиого шунта с гликолизом
|
путь выглядит как цикл. Другой продукт — глнцеральдегид-3-фосфат, включившись в гликолиз, превращается в анаэробных условиях в лактат, а в аэробных сгорает до С02 и Н20. Нетрудно подсчитать, что прн превращении глицеральдегид-3-фосфата до лактата образуется две молекулы АТФ, а при сгорании до С02 и HsO — 20 молекул АТФ. Следовательно, в физиологических условиях, когда пентозофосфатный путь превращения углеводов подключен к гликолизу, можно выразить суммарные уравнения превращения глюкозо- б-фосфата через пентозофосфатный цикл. В анаэробных условиях: 3 Г лю козо- б • фосф ат 4-6НАДФ + + 2Ф„-»- 2Глюкозо-б-фосфат+Лактат + 2АТФ + 6НАДФ • Н8+ЗСО, В аэробных условиях: 3 Гл ю козо-6 -фосфат+6НАД ф + + 20АДФ + 20Ф, -»-
-»- 2Г л нжозо-6-фосфат + 6НАДФ -Н, + 6COj+6Н, 0+20АТФ Казалось бы, энергетическая ценность Такого превращения глюкозо-6-фосфа- та через пентозофосфатный цикл ниже, чем по пути аэробного гликолиза (ведь последний дает максимум 38 молекул АТФ). Однако нужно учесть, что большая доля энергии аккумулируется в НАДФ • Н2. Энергетически б молекул НАДФ • Нг равнозначны! 8 молекулам АТФ. Следовательно, энергетический эффект тот же.
Биологическая функция певтоэофвсфагиого цикла
Биологическая функция пентозофосфатного цикла связана с производством двух веществ —- НАДФ • Н2, являющегося «восстановительной силой» при синтезе различных веществ, и метаболита — рибозо-5-фосфата, использующегося как строительный материал в синтезе различных веществ (см, рис. 52). Перечислим его основные функции:
1) амфкболнческая— ои яаляется путем распада углеводов и одновременно веществ, используемых в синтетических реакциях (НАДФ • Н2 и рибо- зо-5-фосфат);
2) энергетическая, так как при подключении его продуктов (глицераль- дегид-3-фосфат) к гликолизу образуется энергия;,.
3) синтетическая — основная функция, связанная с использованием НАДФ • Нг и рибозо-5-фосфата.
НАДФ • Н2 используется: 1) в обезвреживании лекарств и ядов в моно- окснгеназной цепи окисления эидоплазматической сети печени;
2) в синтезе жирных кислот и других структурных и резервных липидов;
3) в синтезе холестерина и его производных — желчных кислот, стероидных гормонов (кортикостероиды, женские н мужские половые гормоны), витаминов D;
4) в обезвреживании аммиака при восстановительном аминировании.
Рибозо-5-фосфат используется в синтезе гистидина, нуклеозидов н нуклеотидов (нуклеотндмоно-, ди- н трифосфатов), нуклеотидных коферментов (НАД, НАДФ, ФАД, КоА) и полимерных производных нуклеотндов — поли- нуклеотидов (ДНК, РНК, коротких олигонуклеотидвв).
Пентозофосфатный путь превращения углеводов активен прежде всего в тех органах и тканях, в которых требуется интенсивное использование НАДФ • Н2 в реакциях восстановительных синтезов и рибозо-5-фосфата в синтезе нуклеотидов и нуклеиновых кислот. Поэтому высокая активность этого пути отмечается в жировой ткани, печени, ткани молочной железы, особенно в период лактации.(так как необходимо синтезировать жир молока), надпочечниках, половых железах, костном мозге, лимфоидвой ткани. Относительно активны дегидрогеназы пеитозофосфатного шунта в эритроцитах. Низкая активность его наблюдается в мышечной ткани (сердце, *скелетная мышца).
2. Биосинтез углеводов в4 тканях
В тканях и органах человека н животных происходит синтез углеводов. Поскольку исходной структурной единицей для образования других М|> чп- сахаридов и для сборки полисахаридов является глюкоза, рассмотрим возможные пути синтеза глюкозы в тканях и органах. На образование глюкозы из веществ неуглеводной природы указывает тот факт, что при длительном голодании (в лечебных целях или крайних жизненных ситуациях) углеводные запасы резервных нолисахаридов быстро расходуются, а глюкоза в крови циркулирует, снабжая ткани, особенно мозг, энергией.
Глюконеогенез
Синтез глюкозы из неуглеводных источников называется глкнчонеогенезол или новообразованием глюкозы. Он возможен не во всех тканях организма. Главным местом глюкоаеогенез.а является печень. В меньшей степени он протекает в почках, слизистой кишечника.
Механизм глкжонеогенеза. Поскольку в гликолизе имеются три энергетически необратимые стадии на уровне пируваткиназы, фосфофруктокиназы и гексокиназы, то образованна глюкозы нз простых неуглеводных веществ, например пирувата или лактата, путем обратного гликолиза («снизу вверх>) невозможно. Необходимы обходные реакции.
Первый обходный путь при синтезе глюкозы связан с-образова- нием фосфоенолпирувата из пирувата в обход пируваткиназы. Он катализируется двумя- ферментами. Сначала пируват превращается в оксалоацетат. Реакция происходит в митохондриях, куда проникает пируват, и катализируется- пируваткарбоксилазой по уравнению
СНа—С—СООН + НСО7 + АТФ П»Р> 1«™»РЯ°'Ц; '" «3% НООС—СН; —С—СООН + АДФ + н8го4
Этот фермент в качестве кофактора, как и все ферменты, усваивающие COj, содержит биотин. Оксалоацетат поступает из митохондрий в цитоплазму, где протекает глюконеоген$э. В цитоплазме оксалоацетат превращается в фосфо- енолпируват в реакции, катализируемой фосфоеяолпнруват-карбоксилазой:
НООС—CHj—С—СООН -1- ГТФ(АТФ) —, СН, - С—СООН + ГДФ (АД Ф) +СО, О POjHJ
Равновесие реакции сдвинуто вправо. Источником фосфатных групп служит главным образом ГТФ, но может быть и АТФ.
От фосфоенолпирувата до фруктозо-1, 6-бисфосфата все реакции гликолиза обратимы, поэтому образовавшиеся молекулы фосфоенолпирувата используются для образования фруктозо-1, 6-бисфосфата теми же ферментами гликолиза.
Второй обходный путь связан с образованием из фруктозо-1, 6- бисфосфата фруктозо-6-фосфата в обход фосфофруктокиназной реакции. Реакция катализируется фруктоэо-бисфосфатаэой:
Ф р уктозо-1.6-6 и сф Осф ат + Н 80 висфосфатчз» фруктс)30.6-фосфат + Н3РО,
Реакция необратимо сдвинута вправо. Фруктозо-б-фосфат изомеризуется в глюкозо-б-фосфат с помощью глюкозофосфатизомеразы.
• Третий обходный суть связан с образованием из глюкозо-б- фосфата свободной глюкозы в обход гёксокиназной реакции. Эта реакция катализируется глюкозо-6-фосфатаэой:
Гл ю коз о- 6-фосф at + HsO Глюком-6-фосфмм» Глюкоза -с Н, Р04
Свободная глюкоза, образующаяся в этой реакции, поступает нз ткани в кровь. Общая схема глюконеогенеза из пирувата предстаалена на рис. 50. На примере глкжонеогенеза можно видеть экономичность организации путей обмена, поскольку помимо четырех специальных ферментов глкжонеогенеза: пнруваткарбоксилазы, фосфопируваткарбокснлазы, фруктозо-бисфосфатазы и глюкозо-6-фосфатазы для новообразования глюкозы используются отдельные ферменты гликолиза.
Неуглеводные источники для глкжонеогенеза. Субстратами для синтеза глюкозы служат не только пируват или лактат, поступающие в печень и почки, но и другие неуглеводные соединения. Согласно схеме глюконеогенеза (см. рис. 50), можно предсказать, что все вещества неуглеводной природы, которые превращаются или в один из метаболитов гликолиза (первая группа веществ), или в пируват (вторая группа), или в оксалоацетат (третья группа), являются потенциальными источниками новообразования глюкозы. К.веществам первой группы можно отнести глицерин, который превращается в днгидроксиацетонфосфат, а далее в зависимости от условий идет по пути глюконеогенеза или по пути гликолиза. Вовлечение глицерина в глюконе'огеиез происходит по схеме
ГлИЦеролфосфокмнам
1) Глицерин > о -Г л и иеролфосф ат
АТФ АЛФ
а -Глмиеролфосфатлегиарогеиго
2) о -Г ли иеролфосф а т..—. * д и гид роке и ацетон фосфат
f* ^
НАД НАД-Н+Н +
Далее дигияроксияцетонфосфат используется в синтезе глюкозы.
К субстратам глюконеогенеза можно отнести и кислоты цикла Кребса, которые превращаются в оксалоацетат (вещества третьей группы). Однако главными источниками глюконеогенеза являются аминокислоты, превращаю-
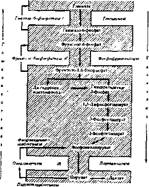 Рнс. 50. Схема глюконеогенеза
Рнс. 50. Схема глюконеогенеза
|
щнеся и в пируват, и в оксалоацетат, а следовательно, и в глюкозу. Аминокислоты, участвующие в новообразовании глюкозы, называются гликогенны- ми. К ним относятся все белковые аминокислоты, кроме лейцина.
Биосинтез гликогена
(г л и ко ген огеяез)
Синтез гликогена осуществляется во всех клетка^ организма (может быть, исключение составляют эритроциты), но особенно активно о~н протекает в скелетных мышиах и печени. Реакция распада гликогена, катализируемая гликогенфосфосфорилааой, почти необратима, поэтому она не участвует в синтезе гликогена. Возможно два варианта его синтеза. Один заключается в наращивании глюкозных единиц иа существующий фрагмент гликогена (затравка гликогена), а другой начинается с молекул глюкозы. Источником остатков глюкозы при синтезе гликогена служит активная форма ее — уридни- дифосфатглюкоза (УДФ-глюкоза), которая образуется из глЮкозо-1-фосфота и УТФ с участием фермента глюкозо-1-фосфат-уридиАТрансферазы по уравнению
Глюкозо-l-фосфат + утФз* УДФ-глюкоза +Н4РаОт
На следующей стадии происходит перенос остатка глюкозы с УДФ-глюкозы на затравку гликогена с помощью фермента гликогенсинтетазы:
УДФ-глюкоза + (Глюкоза)„-> -УД Ф +■ (Глюкоэа)„+1
Причем гликогеисинтетаза катализирует образование только а-I—4-гликозид- ных связей. «Ветвящий» фермент — амило- (а-1, 4 -*■ а-1, б)-трансгликозилаза переносит короткие фрагменты (по 2—3 глюкозных остатка) с одного участка гликогена на другой и образует а-1 -»6-гликозидные связи (точки ветвления). Путем чередования действия этих двух ферментов наращивается молекула гликогена.
Если синтез начинается с молекул глюкозы, то сначала происходит перекос остатков глюкозы с УДФ-глюкозы на промежуточный акцешир — Оили- холфосфат (полипренолфосфат). На долихолфосфате синтезируется олигоса- харид, который затем переносится на белок. Достраивание олигосахаридных цепей до молекулы гликогена происходит так же, как и в первом варианте. О приемлемости второго варианта синтеза гликогена говорит то, что гликоген всегда связан с небольшим количеством белка.
Взаимоотношение процессов синтеза и распада гликогена. Гликогеисинтетаза существует в двух формах, переходящих одна в другую. Фосфорилиро- ванная, или неактив(шя, форма ее называется гликогеисинтетаза D, нефос- форилированная, или активная, форма — гликогеисинтетаза I. Переход из одной формы в другую осуществляется с помощью двух ферментов — киназы гликогенсинтетазы (1) и фосфатазы гликогенсинтетазы (2) по уравнениям:
АТФ АД»
Гликогеисинтетаза I i Глигогенсинтепм D
(неф осф ори ли ро-, ^ ' —•**" < ф осф ор или ро ванн ы й МННЫЙ фермент) f 2 фермент)
К, Р04
Процессы синтеза и 'распада гликогена в клетках регулируются благодаря включению механизмов фосфорилирования ключевых ферментов обмена гликогена — гликогенсинтетазы и гликогёнфосфорнлазы. Активация аденилатци- клазы (например, под действием адреналина или глюкапона) приводит к образованию цАМФ, запускающего «каскадный» механизм фосфорилирования гликогенсинтетазы н гликогёнфосфорнлазы, что приводит, к образованию неактивной (фосфорилированной) гликогенсинтетазы D и активной (фосфори- лированНой) гликогёнфосфорнлазы А. Эта ситуация благоприятствует распаду гликогена. Напротив, включение механизма дефосфорилирования указанных ферментов с помощью фосфопротендфосфатазы приводит к образованию неактивной гликогёнфосфорнлазы В н активной гликогенсинтетазы I, что способствует синтезу, а не распаду гликогена.
Биосинтез других олнгосахаридов и полисахаридов
Гомо- и гетерополисахариды входят в качестве углеводного компонента в плазменные и структурные гликопротеиды млекопитающих. Эти углеводы образуются из небольшого ассортимента моносахаридов: галактозы, маннозы. N-ацетилглюкозамина, N-ацетилгалактозамнна, фукозы, ейаловой кислоты. Полисахариды соединительной ткани содержат глюкуроновую кислоту, ндуро- новую кислоту, ксилозу и сульфатированные производные N-ацетил глюкоза- мина или N-ацетилгалактозамина. Для сборки этих гомо- и гетерогликанов необходимы активированные формы моносахаридов в виде нуклеозидфосфат- производных моносахаридов. - Для синтеза используются УДФ-производные глюкозы, галактозы, N-ацетилглюкозамина, N-ацетилгалактозамина, глюкуро- новой кислоты и ксилозы; ГДФ-производные макнозы и фукозы; ЦМФ-произ- водные сиаловой кислоты. Образование большинства нуклеозидфосфатсаха- ров происходит путем взаимодействия моносахаридов или их производных с соответствующими нуклеозидтрифосфатами. В некоторых случаях образование одних моносахаридов из других происходит в составе нухлеознддифосфат- сахаров. Например, из УДФ-глюкозы образуется УДФ-глюкуроновая кислота и УДФ-ксилоза:
УДФ-глюкоза—^^ УДФ-глюкуроновая кислота ■ ^ > УДФ-ксило»
2ЧАД + 2 Н АЛ-Н 2 СО]
Из ГДФ-маннозы'образуется ГДФ-фукоза:
ГДФ-манном ГДФ-фукоза + HjO
НАДФ' НАДФ Н2
Следует отметить, что, например, УДФ-глюкуроновая кислота образуется в тканях не только для синтеза полисахаридов, но и для обезвреживания и выведения токсических или бесполезных для организма веществ и чужеродных соединений, попадающих в организм.
Синтез олигосахаридов происходит с участием специфических еликозил• трансферов, от разнообразия и специфичности действия которых в каждой клетке зависит образование того или иного типа гомо- или гетероглнкаяа. Гликозилтрансферазы связаны в клетках с мембранами эндоялазматической сети или аппарата Гольджи, где и происходит наиболее активно сборка олигосахаридов. Первоначально сборка, очевидно, идет на молекуле полипре- нолфосфата, на который гликозилтрансферазы последовательно переносят моносахарндные остатки от нуклеозидфосфатсахаров. Затем синтезированный олигосахарид переносится на белок с образованием гликопротеидов. Возможны сразу перенос гликозильных остатков и сборка олиго- и полисахаридов ма белковой основе.
3. Регуляция обмена углеводов в организме
Интенсивность рассмотренных путей превращения углеводов в разных тканях организма неодинакова и определяется особенностями обмена каждой ткани и органа. Однако в условиях целого организма некоторая специализация путей превращения углеводов -в отдельных тканях удачно дополняет друг друга. Например, при активной мышечной работе требуется энергия, которая первоначально извлекается в ходе распада гликогена до молочной кислоты. Последняя вымывается в кровь, с которой поступает в печеночную ткань, где из нее образуется глюкоза в. ходе глюконеогенеза. Глюкоза из печени с кровью достигает скелетных мышц, где расходуется на образование энергии и откладывается в виде гликогена. Этот межтканевый (или межорганный) цикл в обмене углеводов получил название цикла Кори:
Наиболее важное значение для организма имеет поддержание на постоянном уровне глюкозы в крови, поскольку глюкоза является основным энергетическим субстратом для нервной ткани. В норме содержание глюкозы в крови составляет 3, 3—4, 0 ммоль/л. Повышение ее в крови называется гипергликемией. Если гипергликемия достигает 9—10 ммоль/л. то глюкоза выделяется с мочой, т. е. наступает глюкозурия. Снижение содержания глюкозы в крови называется гипогликемией. Если гипогликемия достигает порядка 1, 5 ммоль/л, то возникает обморочное состояние, а если еще ниже, то повышается возбудимость нервной системы вплоть до судорог.
Для понимания механизма регуляции уровня глюкозы в крови необходимо рассмотреть процессы, которые способствуют его повышению» или понижению (рис. 54).
Процессы, ведущие к гипергликемин:
J) всасывание глюкозы из кишечника (пищевая гяпергликемня);
2) распад гликогена до глюкозы (как правило, в печени);
3) глюконеогенез (в печени и почках).
Процессы, ведущие к гипогликемии:
1) транспорт глюкозы из крови в ткани и окисление ее до конечных продуктов;
2) синтез из глюкозы гликогена в печени и скелетных мышцах;
3) образование из глюкозы триацнлглицерина в жировой ткани.
Прием углеводов с пищей вызывает скоропреходящую (через 1—2 ч) гипергликемию, а иногда и глюкозурию. Голодание приводит к мобилизации запасов гликогена в печени и скелетной, мышце, что препятствует развитию гипогликемии, но лишь.» течение нескольких часов. Затем при продолжительном голодании уровень глюкозы поддерживается только благодаря новообразованию глюкозы, главным образом за счет аминокислот белков, распадающихся в тканях. По существу, резервами белков, расходующихся на образование глюкозы, определяется потенциальная возможность выдержать срок голодания.
| Глюкоиеогенез— |
| Рис, 51. Схема процессов, повышающих (слева) н понижающих (справа) уровень глюкозы в крови |
Уровень глюкозы в крови находится под контролем нервно-гормональных механизмов. Возбуждение симпатического отдела вегетативной нервной системы повышает уровень глюкозы в крови, а парасимпатического, — снижает. Единственным гормоноц снижающим содержание глюкозы, является инсулин. Он стимулирует все три процесса усвоения глюкозы (транспорт внутрь клеток и ее
9—271
распад, синтез гликогена, синтез триацилглицерина из глюкозы в жировой ткани). Все остальные гормоны повышают уровень глюкозы, поэтому их иногда называют контринсулярными. К ним относятся адреналин, глюкагон, тироксин и трииодтиронин, соматотропин (стимулируют распад гликогена), глюкокортикоиды (стимулируют глюконеогенез).
ГЛАВА 18. ОБМЕН ЛИПИДОВ
В тканях организма происходит непрерывное обновление липидов. Основную массу липидов тела человека составляют триацнлглицерины, которые имеются в виде включений в большинстве тканей, но особенно ими богата жировая ткапь, почти полностью состоящая ич трианилглицеринов. Поскольку они играют энергетическую роль, то процессы обновления трнглицеридоа (период полупревращения их в разных органах колеблется от 2 до 18 сут) связаны с мобилизацией и депонированием их в процессе образования энергии.
Сложные липиды (фосфолипиды, сфинголипиды, гликолипиды, холестерин и его эфиры), входящие в состав биологических мембран, обновляются ченее интенсивно, чем триацил глицерины. Их обновление связано или с восстановлением поврежденного участка мембраны, или с заменой «дефектной» молекулы на новую.
Обновление липидов тклней требует предварительного внутриклеточного гидролиза их ферментами.
1. Распад липидов в тканях Внутриклеточный гидролиз липидов Гидролиз триацилглицеринов в тканях осуществляется тканевой триацилгли- церинлипазой, которая гидролизует их на глицерин и свободные жирные кислоты. Имеется несколько разновидностей тканевых липаз, отличающихся прежде всего оптимумом рН и локализацией в клетке. Кислая липаза содержится в лизосомах, щелочная — в микросомах, нейтральная — в цитоплазме- Характерным свойством тканевой липазы является чувствительность к гормонам, которые, активируя аденилатциклазу, вызывают переход неактивной липазы тканей в активную путем фосфорилироваиия с помощью протеинкина- зы, Механизм этот сходен с активированием фосфорилазы В. Под действием липазы происходит мобилизация триацилглицеринов- Этот процесс называется также тканевым липолизом.